Texte original rédigé par Ana Mingorance disponible ici en Anglais
Depuis dix ans, la Fondation Loulou organise une rencontre annuelle, le Forum CDKL5, où les scientifiques et développeurs de médicaments travaillant sur le trouble déficitaire en CDKL5 (CDD), ainsi que des représentants d’organisations de patients, se réunissent pour discuter des derniers développements dans le domaine et pour avancer vers des traitements et des remèdes. Vous pouvez trouver des résumés de quelques-unes des dernières rencontres ici : 2018, 2019, 2020, 2021, 2022 et 2023.
L’édition 2024 du Forum CDKL5 a eu lieu du 28 au 29 octobre à Boston, et se tiendra également à Boston l’an prochain pour l’édition 2025. Ce fut le plus grand Forum à ce jour, avec plus de 200 participants, dont des représentants de 33 entreprises et 18 groupes nationaux de patients. C’était aussi une édition spéciale, car c’était le 10ᵉ Forum CDKL5 (le premier ayant eu lieu il y a 9 ans). Je vais essayer de résumer les principaux messages de cette année. Cela ne couvrira pas toutes les présentations, mais se concentrera plutôt sur les principaux thèmes et les principales avancées — qui sont toujours nombreuses.
1 – Nouvelles découvertes intéressantes sur la biologie du CDKL5 et le CDD

Image : La chercheuse Maria del Carmen Martin Carrascosa (CIPF), le directeur du Forum Dan Lavery (de la Fondation Loulou) et la docteure en recherche Josephine Thinwa (UTSouthwestern).
Sila Ultanir a introduit une session sur la biologie du CDKL5 en disant qu’il y a quelques années, on savait seulement que le CDKL5 était manquant, donc on envisageait uniquement de remettre le CDKL5 pour guérir la maladie. Mais aujourd’hui, nous en savons beaucoup plus sur ce qu’il fait dans les cellules, ce qui ouvre différentes possibilités pour essayer de corriger certains aspects de la maladie sans avoir besoin de remettre le CDKL5 pour l’instant.
Nous avons appris d’Oguz Kanca de Baylor que certains patients avec des mutations de gain de fonction dans CDKL1 et CDKL2 présentent des syndromes neurodéveloppementaux, donc CDKL5 n’est pas le seul gène important dans cette famille. Et nous avons appris de Maria del Carmen Martin Carrascosa que les mouches sans CDKL5 présentent des crises d’épilepsie spontanées et des stéréotypies répétitives, ce qui semble mieux capturer le manque de CDKL5 que chez les souris. Cependant, chez tout animal apparu dans l’évolution avant l’apparition des mâchoires (oui, les mâchoires), CDKL5 agit presque comme un CDKL1-4 qui n’a pas toutes les fonctions de notre CDKL5.
L’un de ces gènes CDKL potentiellement redondants est CDKL2, donc l’année dernière, nous avons envisagé si l’augmentation de CDKL2 pourrait être une approche thérapeutique possible en l’absence de CDKL5. Cette année, Kevin Dempster a présenté ce qui se passe si on obtient une souris sans CDKL5 ni CDKL2… Est-ce que cela s’aggrave encore ? La réponse est oui, mais de manière intéressante, CDKL2 semble ne faire que certaines des fonctions de CDKL5 dans la cellule, pas toutes, notamment pas le travail de modifier l’activité des canaux calciques et des récepteurs de glutamate. Donc, en quelque sorte, augmenter CDKL2 a le potentiel de corriger certaines des conséquences de l’absence de CDKL5, mais d’autres conséquences doivent encore être traitées séparément, comme le besoin d’inhiber Cav2.3 (plus de détails à ce sujet plus tard).
Sur le plan de la biologie, nous avons appris de Josephine Thinwa que les patients atteints de CDD pourraient être plus sensibles aux infections virales, causant une réponse inflammatoire plus importante, et de Lauren Orefice que le manque de CDKL5 dans différents neurones sensoriels rend les personnes atteintes de CDD plus sensibles aux textures, sensations (sensibilité tactile, comme une étiquette sur vos vêtements) et plus enclines aux douleurs gastro-intestinales. Tous ces éléments semblent être des problèmes sensoriels causés par le manque de CDKL5 dans les neurones sensoriels.
2 – Au-delà de la boîte à outils de recherche : l’année des plateformes
a. Cellules et souris
L’un des principaux objectifs de la Fondation Loulou dès le départ était de s’assurer que tout scientifique, où qu’il soit dans le monde, puisse travailler sur le CDD. Cela signifiait créer une collection d’outils de recherche comme des modèles animaux et les rendre accessibles en open source. Peut-on voir où se trouve CDKL5 dans cette cellule ? Peut-on voir s’il est actif ? Peut-on voir les conséquences de l’absence de CDD ? Et qu’est-ce que cela signifie pour la physiologie de cet organe ? Nous ne pouvons pas répondre à cela sans cellules, anticorps et souris.
Cela a mené à une collection croissante de modèles animaux, de modèles cellulaires et d’anticorps qui sont disponibles pour la communauté. Mais cette année a peut-être été celle de la « plateform as a service», qui est l’étape suivante une fois que les outils existent.
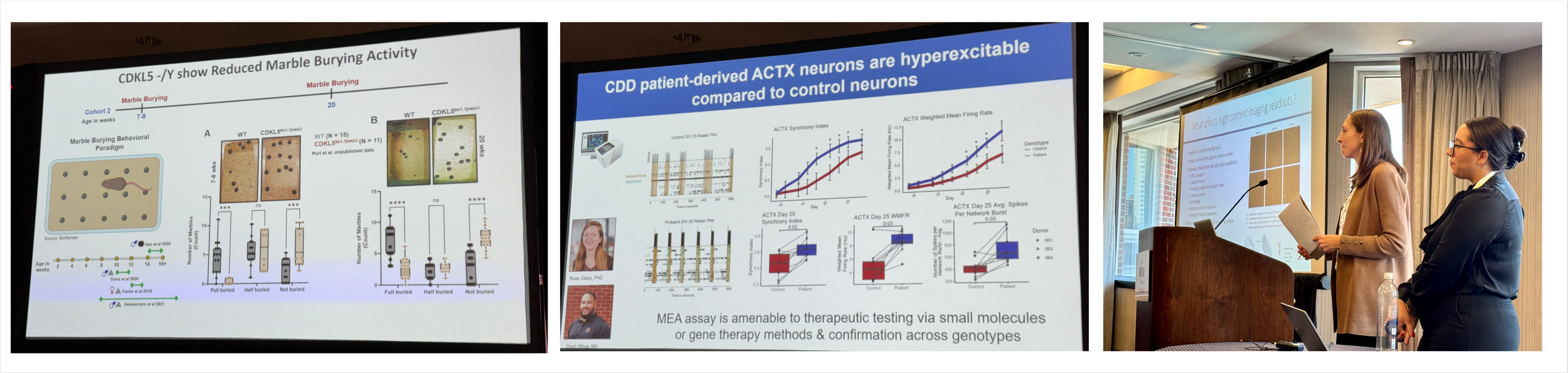
Image : diapositive de la plateforme de test pour les souris atteintes de CDD, diapositive de la plateforme de neurones dérivés d’iPSC atteints de CDD, et chercheuses Liz Buttermore (BCH) et Jasmine Carter (Fondation Loulou) lors de la session de discussion sur les cellules iPS.
Je tiens à souligner les neurones dérivés d’iPSC de patients atteints de CDD, qui fonctionnent comme un service au Boston Children’s Hospital Neuron Core dirigé par Liz Buttermore, et la session de discussion dirigée par Liz et Jasmine Carter de la Fondation Loulou à propos des modèles dérivés d’iPSC.
Liz nous a fait parcourir tout le travail acharné qui a permis de développer un très bon test d’épilepsie in vitro avec des lignées d’iPSC dérivées de patients, et c’était un excellent exemple de la difficulté à standardiser un test de ce type pour le rendre robuste et fiable. Les entreprises peuvent maintenant envoyer leurs composés à Boston pour les tester dans ce modèle CDD « d’épilepsie en boîte » utilisant des réseaux de microélectrodes.
Nous avons eu une session de discussion l’après-midi dirigée par Liz et Jasmine pour voir comment la communauté académique et biotechnologique souhaiterait collaborer pour mettre en place ces modèles in vitro. Il y a eu des discussions sur l’apprentissage mutuel des succès et des erreurs, et sur le fait d’avoir un canal partagé pour poser des questions car résoudre les problèmes de ces modèles peut devenir très compliqué. La discussion était fantastique (et je suis désolé d’avoir manqué les sessions de discussion parallèles).
Tout comme pour les cellules, le Jackson Labs a mis en place un panel de modèles de souris de maladies neurodéveloppementales qui sont désormais disponibles pour les tests de médicaments sous forme de service payant. Rajat Puri a présenté des données sur leur service de test préclinique pour les souris atteintes de CDD, montrant des résultats solides pour différents âges de souris, lots de souris et même d’un chercheur de laboratoire à l’autre. Encore une fois, ces normes sont très difficiles à maintenir, et c’est puissant de les avoir disponibles en tant que service au lieu de devoir tout résoudre dans chaque laboratoire. Les tests que j’ai préférés montraient à quel point les souris atteintes de CDD sont incapables d’enterrer des billes ou de construire des nids, ce qui est l’équivalent chez les souris des activités de la vie quotidienne pour les humains.
Et pourquoi ces services sont-ils si importants pour les entreprises travaillant sur les traitements ? Parce qu’avoir une souris ou une lignée cellulaire disponible, c’est comme acheter des ingrédients au supermarché, on doit encore les « cuisiner » dans le laboratoire, mais ces modèles in vitro de patients et ces modèles comportementaux complexes chez les souris sont très élaborés et faciles à mal maîtriser, donc les avoir disponibles sous forme de service revient à proposer des restaurants où l’on peut obtenir le plat complexe déjà prêt. Il est bien plus facile d’aller dans un restaurant et de commander une paella que de passer deux ans à apprendre à bien la cuisiner.
b. Patients
Il existe une étude clinique observationnelle sur le CDD conçue pour comprendre les échelles cliniques permettant de mesurer des symptômes autres que les crises dans les essais, et pour collecter des données qui pourraient servir de référence pour de futurs essais cliniques sur le CDD. Elle s’appelle l’étude CANDID, et j’en suis très fier, non seulement parce que j’ai fait partie de l’équipe initiale qui a perçu la nécessité d’une telle étude et l’a lancée, mais aussi parce qu’elle a évolué et appartient désormais à la communauté. Au Forum, Xavier Liogier de la Fondation Loulou a présenté les résultats des évaluations des échelles dans l’étude CANDID, qui comprend plus de 100 patients des États-Unis, de l’UE et de la région MENA. Nous avons appris non seulement quelles échelles pourraient être utilisées aujourd’hui dans un essai pour une thérapie génique, mais aussi le fait que 83 % des patients seraient éligibles pour un essai s’il demandait un minimum de 16 crises par mois. 83 %, c’est énorme ! Dans d’autres syndromes, 25 % ou moins des patients auraient suffisamment de crises pour participer aux essais, et les crises resteront probablement le critère principal dans les essais, donc d’une certaine manière, nous avons la maladie parfaite pour les essais cliniques. C’est important de le savoir !

Image : Xavier Liogier (Fondation Loulou) présente une mise à jour sur CANDID, et discussion de groupe avec des médecins et des représentants des patients.
Il y a également eu une réunion pour l’étude CANDID où Xavier et Maria Makarovskaya, les deux professionnels de la Fondation Loulou en charge de CANDID, ont demandé aux cliniciens de l’étude et aux représentants de la communauté de patients leur expérience dans l’étude et leurs retours. Et c’est là que j’ai réalisé que CANDID a été lancée par un petit groupe de personnes, mais qu’elle est désormais entre les mains d’un groupe beaucoup, beaucoup plus large, y compris les 112 patients inscrits et leurs parents, ainsi que tous les chercheurs de l’étude et leur équipe d’infirmières et de psychologues. C’est énorme et c’est une grande source de fierté pour beaucoup.
Il y a également un grand effort sur les biomarqueurs dans les fluides corporels qui a été discuté dans l’une des sessions de discussion. Un biomarqueur dans un fluide est un moyen de mesurer quelque chose dans le sang, le LCR ou un autre fluide corporel, montrant qu’une thérapie fonctionne. Par exemple, le taux de sucre dans le sang est un biomarqueur pour le diabète, tandis que le cholestérol dans le sang est un biomarqueur pour le risque cardiovasculaire. Maurizio Giustetto, d’Italie, explore la salive pour mesurer de petites vésicules que les neurones émettent pour communiquer entre eux et qui pourraient potentiellement être recueillies dans la salive (incroyable !). Il existe aussi une collaboration internationale appelée ELPIS dirigée par Massimiliano Bianchi, qui collecte des échantillons de sang de patients pour rechercher d’éventuels biomarqueurs dans le plasma. Ils ont déjà trouvé des biomarqueurs potentiels dans le plasma, j’en ai parlé l’année dernière, et un an plus tard, le programme s’étend à d’autres pays et envisage une collecte d’échantillons de sang et de salive de patients et de leurs frères et sœurs (comme témoins) lors de la conférence des patients à Rome en 2025. Restez à l’écoute pour plus d’informations à ce sujet.
3 – Thérapies : le présent, le proche avenir et le futur flou
Au début de la session sur les thérapies, Omar Khwaja, qui est un médecin ayant traité des enfants atteints de maladies neurodéveloppementales et qui est ensuite devenu développeur de médicaments, a donné un aperçu du pipeline de la CDD aujourd’hui.
Nous avons le ganaxolone approuvé aux États-Unis et en Europe, et les patients atteints de CDD utilisent également souvent l’Epidiolex en dehors des indications, car il est approuvé pour le LGS et qu’il y a de bonnes données de Phase 2 pour la CDD. Nous avons donc « presque » deux médicaments approuvés. Nous avons ensuite des essais cliniques avec le fenfluramine (en Phase 3) et le bexicaserin (sur le point de commencer la Phase 3 pour les DEEs, y compris la CDD). Après cela, il y a un groupe de quatre programmes « presque prêts pour l’essai », dont trois thérapies géniques.
Selon Omar, nous avons fait un grand chemin en ces 9 années depuis le premier Forum, avec un paysage complet de programmes en développement, y compris des thérapies géniques modifiant la maladie en phase préclinique avancée et plusieurs médicaments en essais ou approuvés. Je vous invite tous à consulter les anciens résumés du Forum pour voir ces progrès, y compris les anciens essais qui n’ont pas progressé, comme l’ataluren (données négatives en Phase 2) et le soticlestat (données positives en Phase 2 mais non retenues par la pharmacie pour une Phase 3).
a. Le présent

Images : Sabine Bongardt de UCB Pharma, Randall Kaye de Longboard, et une diapositive de la présentation d’Elisa Borghi sur l’essai de suppléments prébiotiques et probiotiques.
UCB Pharma a présenté les progrès de l’essai de Phase 3 avec le fenfluramine dans la CDD, qui devrait probablement clôturer le recrutement à la fin de cette année. Ils demandent particulièrement aux enfants âgés de 1 à 2 ans de participer, avec environ 20 places disponibles dans l’essai. C’est très exceptionnel, car les essais ne commencent souvent qu’à 2 ans, et dans une maladie comme la CDD qui peut commencer dès les premières semaines de vie, ces deux ans peuvent signifier plus de mille crises avant que l’enfant puisse commencer à prendre du fenfluramine (ou tout autre médicament ayant un âge minimum de 2 ans !). Donc, si vous connaissez une famille avec un enfant d’un an atteint de CDD et ayant des crises incontrôlées, veuillez leur faire savoir à propos de cet essai (plus d’informations sur les lieux sur le site de l’essai) afin que cet essai puisse compléter le recrutement à la fin de l’année.
Et alors qu’un essai se termine, un autre commence. Longboard Pharma développe un médicament appelé bexicaserin, qui est un fenfluramine de deuxième génération, et il commence un essai de Phase 3 combinant tous les syndromes épileptiques et en particulier les plus importants (y compris la CDD) pour des patients âgés de 2 à 65 ans ayant au moins 4 crises comptables par mois. Ils visent 80 hôpitaux d’essai, potentiellement plus de 100, et commenceront à recruter très bientôt. Donc, vérifiez avec vos médecins si Longboard les a contactés à propos de cet essai à venir avec bexicaserin appelé DEEp OCEAN.
Au fait, Longboard a été assez populaire récemment en choisissant de combiner tous les syndromes épileptiques (tous les DEEs) en un seul essai et ils ont même récemment été achetés par Lundbeck, la société pharmaceutique qui fabrique le clobazam. Donc, il y a eu beaucoup de dynamisme autour du bexicaserin. Et Longboard a reçu le prix « 2024 CDKL5 Forum Company Making a Difference Award » et le CMO Randall Kaye a parlé de voir une lumière ambrée comme un signe pour accélérer, et non pour s’arrêter. Longboard accélère vers des traitements pour tous les DEEs, même si la difficulté de la tâche à venir aurait pu amener d’autres à vouloir ralentir (ou à se détourner). Pour nous, en CDD, leur Phase 3 signifie une autre chance d’accéder à une nouvelle molécule en développement avant qu’elle ne soit approuvée.
Et lors du Forum, nous avons également eu une présentation très intéressante d’Elisa Borghi sur un essai clinique avec un mélange de suppléments prébiotiques et post-biotiques, donc « nourriture pour votre microbiome » et « produits que le bon microbiome libérerait ». Leur recherche a été lancée par le groupe de familles de patients italien, et elle est maintenant en essai de Phase 2 avec des patients atteints de CDD pour voir comment cela pourrait améliorer la fonction gastro-intestinale et l’épilepsie, qui semble avoir un composant gastro-intestinal. Ce que j’aime dans ce programme, c’est que si l’essai est positif, les familles peuvent accéder directement au supplément et n’ont pas besoin d’attendre des approbations réglementaires longues et des négociations de remboursement des prix, comme c’est le cas pour les médicaments. Et il y avait une autre entreprise présente, bien qu’elle ne présente pas, qui cible également le microbiome, mais en utilisant les bonnes bactéries (donc ce n’est pas un pré- ou post-biotic mais un traitement biologique !). J’espère que l’année prochaine, nous pourrons également les entendre et en savoir plus sur les interventions cliniques dans ce domaine intestin-cerveau.
b. Le proche avenir
Je ne sais pas si vous avez réalisé que nous avons maintenant trois thérapies géniques et un programme de petite molécule tous passés à la nomination de candidat clinique. « Candidat clinique » est comment nous appelons un médicament ou une thérapie qui a déjà été optimisé et ajusté, et que les scientifiques vont ensuite transférer aux tests de sécurité et de toxicologie chez des animaux autres que les souris pour se préparer à déposer une IND (une autorisation pour commencer les essais).

Images en haut : Emil Kakkis d’Ultragenyx et diapositive de leur programme de thérapie génique. Diapositive de Lario Therapeutics.
Images en bas : diapositive de thérapie génique d’UCDavis et Kyle Fink. Diapositive de la présentation de thérapie génique de la Loulou Foundation et Penn.
L’une de ces thérapies géniques est celle d’Ultragenyx, que le PDG Emil Kakkis explique qu’elle atteint déjà un nombre suffisant de neurones chez les porcs (et est sûre) pour être prête pour les essais, mais ils souhaitent encore passer un peu de temps à voir s’ils peuvent faire mieux. Emil nous a rappelé que « le cerveau est plus plastique et plus capable que nous ne le pensons ».
Un deuxième programme dans cette catégorie du proche avenir est la thérapie génique de la Loulou Foundation, financée par sa filiale Elaaj et créée par le programme de thérapie génique de l’UPenn sous la direction de l’expert en thérapie génique Jim Wilson. Jim a récemment quitté Penn pour fonder une entreprise appelée Gemma Therapeutics, donc la présentation de cette thérapie génique a été faite par Janine Lamonica, la scientifique principale de ce programme chez Gemma, et elle a également montré une thérapie génique qui semble prête pour les essais une fois que l’équipe est convaincue qu’elle ne peut pas faire mieux. Les thérapies géniques d’Ultragenyx et de la Loulou Foundation utilisent une copie du gène humain CDKL5 dans un virus associé à l’adénovirus (AAV) et sont administrées par injection dans la cisterna magna, la grande piscine de LCR que l’on peut accéder à la nuque, entre le cou et le crâne (via ICM). Donc, ces thérapies géniques sont assez similaires.
Une troisième thérapie génique qui passe maintenant à la toxicologie est l’approche de réactivation CRISPR 2.0 de Kyle Fink à UCDavis qui utilise un CRISPR modifié pour trouver le deuxième gène CDKL5 dans les cellules, qui est inactivé dans le cadre du chromosome X inactif, et fait en sorte que la cellule le lise. Au lieu de chercher et de couper, il s’agit d’un CRISPR de type chercher et activer, et pour l’acheminer vers les neurones, les scientifiques utilisent deux virus AAV, chacun portant la moitié de la séquence CRISPR (en fait des millions de virus de chaque, pas seulement un de chaque, pour que lorsqu’ils infectent le même neurone, ils puissent faire le type de CRISPR chercher et activer). Leurs données de sauvetage de souris sont magnifiques et ils constatent du succès chez des souris femelles adultes, montrant encore une fois qu’il n’est probablement jamais trop tard pour la CDD !
Et le programme de petite molécule qui a déjà nommé un candidat (une molécule finale) est le programme d’inhibiteur de Cav2.3 de Lario Therapeutics. Il y a deux ans, nous avons appris que Cav2.3 est un canal qui fait tirer les neurones de glutamate et qui est généralement contrôlé par CDKL5 comme un frein, réduisant son activité.
En l’absence de CDKL5, Cav2.3 est trop actif et les neurones excitateurs deviennent fous, donc nous aurions besoin d’inhibiteurs. L’année dernière, nous avons vu des données préliminaires sur ces inhibiteurs fabriqués par Lario, et cette année, ils nous ont montré une belle activité dose-réponse dans des neurones glutamatergiques dérivés de lignées cellulaires de patients atteints de CDD, donc plus il y a de médicament, plus la correction de l’excitation excessive est importante. C’est un médicament, pas une thérapie génique, ce qui le rend très attrayant à combiner avec d’autres traitements.
c. L’avenir flou
C’est ici que nous avons toutes les autres thérapies, y compris l’édition génique (celle qui corrige votre séquence d’ADN, par David Liu), ou la thérapie génique qui corrige les mutations non-sens (par Tevard), ou les approches ASO (oligonucléotide antisens) en phase précoce qui tentent de sauver CDKL5 ou d’augmenter CDKL2, et même les efforts pour fabriquer la protéine CDKL5 en laboratoire pour ensuite l’injecter dans le cerveau (thérapie de remplacement enzymatique). Il y a également des discussions sur le changement de type de virus pour ceux qui peuvent être administrés par injection dans le sang et ensuite traverser vers le cerveau, afin que nous n’ayons pas besoin d’injecter les thérapies géniques directement dans le cerveau. Beaucoup de gens travaillent dur sur toutes ces pistes, mais nous ne savons pas SI l’une d’elles parviendra un jour aux essais ni QUAND elles pourraient parvenir aux essais. Ce que nous savons, c’est qu’aujourd’hui, le meilleur type de thérapie génique que la médecine sait réaliser est de placer une copie de gène à l’intérieur d’un virus AAV9 ou similaire et d’administrer cette thérapie génique directement dans le cerveau, comme les trois thérapies géniques pour le CDD dans la catégorie « proche ». Tout le reste reste un avenir flou (mais plein d’espoir).
4 – Qu’est ce qui est suffisant
Une chose qui est devenue claire lors des discussions avec les intervenants et le panel de l’industrie est que, comme les thérapies géniques AAV ne peuvent être administrées qu’une seule fois, nous devons vraiment nous assurer que nous avons la bonne dose et la bonne distribution avant de commencer les essais. Dans d’autres maladies où le principal type de « thérapie génique » est un oligonucléotide antisens (ASO), qui est comme un morceau d’ADN que vous injectez dans la colonne vertébrale tous les quelques mois, vous pouvez commencer les essais plus tôt et déterminer la bonne dose plus tard. Mais cela ne peut pas être fait avec des thérapies livrées par virus, qui sont une fois et c’est tout. Je vais vous donner deux exemples réels pour illustrer cet avantage de rapidité pour aller aux essais avec les ASOs : (1) dans le syndrome d’Angelman, Ultragenyx est entré dans la clinique avec une dose d’ASO initiale trop élevée, ils ont observé une inflammation localisée dans la colonne vertébrale et une paralysie des jambes inquiétante, mais cela était transitoire, et ils ont pu continuer à administrer des doses plus faibles à ces mêmes patients. (2) Dans le syndrome de Dravet, Stoke Therapeutics a commencé les essais en pensant que la bonne dose serait de 30 mg, ce ne fut pas le cas, donc ils ont augmenté à 45 mg pour essayer de voir l’efficacité, ce qui n’était toujours pas suffisant. Ils ont finalement commencé à utiliser 70 mg comme dose et ont finalement obtenu une efficacité impressionnante. Dans ces deux cas, la première dose était « erronée », mais ce n’était pas un gros problème car on continue à administrer des ASOs tous les quelques mois, donc on peut toujours monter ou descendre. Mais dans le CDD, nous n’avons pas eu de bonnes chances jusqu’à récemment d’utiliser des ASOs, et nous utilisons plutôt des thérapies géniques livrées par virus comme nos premières thérapies géniques, et parce que dans ces cas, vous n’avez littéralement qu’une seule chance, nous prenons beaucoup plus de temps pour commencer les essais car ils doivent être corrects dès le départ.
Alors, comment savons-nous quand c’est suffisant ? Dans le cas du CDD, le principal défi semble être d’être confiant que nous atteignons suffisamment de neurones, car les souris ont de petits cerveaux qui sont faciles à couvrir avec le virus, mais nous avons des cerveaux beaucoup plus grands (un enfant de 5 ans a un cerveau 2 500 fois plus grand que celui d’une souris). C’est donc notre défi, d’avoir suffisamment de virus réparti dans le cerveau des porcs et des singes (cerveau de taille intermédiaire) pour que nous puissions faire confiance au fait que nous pouvons passer aux humains et obtenir suffisamment d’infection cérébrale pour voir une bonne efficacité.
Il y a eu beaucoup de débats sur ce qui est « suffisant » pour passer ces thérapies géniques aux essais, la réponse consensuelle étant que nous devons être « confortablement sûrs » avant de commencer les essais. Il semble toujours que cela arrivera dans un avenir proche, mais c’est pourquoi il est si difficile de déterminer exactement quand. Et les retours des experts de l’industrie dans le panel étaient que, même si nous savons que l’avenir apportera de meilleures thérapies géniques que les plus avancées actuelles, cela ne devrait pas nous empêcher de commencer les essais avec celles qui sont presque prêtes dès qu’elles le sont. Parce que les patients n’ont pas beaucoup de temps à attendre, en particulier s’ils sont jeunes, et parce que nous ne savons pas quelles technologies futures nous apporteront et quand.
Alors que j’écris cela, je pense aussi que nous devons travailler dur pour faire avancer les thérapies non virales vers les essais, car elles peuvent être combinées avec les thérapies géniques virales, alors que les scientifiques n’ont pas encore trouvé un moyen d’administrer plus d’une thérapie génique virale à la même personne (le problème du « redosing », voir aussi la section suivante). Il existe des projets qui n’ont pas été présentés au Forum car ils sont à un stade précoce, mais qui répondent très bien à ce besoin, comme le développement d’ASOs pour augmenter le CDKL2, d’ASOs pour corriger le CDKL5, et la fabrication de l’enzyme CDKL5 en laboratoire pour ensuite la diffuser dans le cerveau (thérapie de remplacement enzymatique). J’espère que nous pourrons les examiner l’année prochaine.
5 – Comment la communauté des patients peut aider

Image : Industry panel, from left to right: Ralf Schmid (Novartis), Sharyl Fyffe-Maricich (Ultragenyx), Randall Kaye (Longboard), Brian Moseley (UCB) and moderator Majid Jafar (Loulou Foundation)
Nous avons eu un panel avec des experts de l’industrie dans le développement de médicaments et de thérapies géniques pour voir comment nous, la communauté, pouvons aider à faire avancer les nouveaux traitements plus rapidement. Voici quelques messages :
ÉDUQUER/RECHERCHE : Aidez les familles à comprendre que participer à la recherche devrait faire partie du paradigme de traitement. Cela ne doit pas nécessairement être entrer dans des essais cliniques avec des médicaments, mais peut-être des études cliniques d’observation comme CANDID ou des études de biomarqueurs comme ELPIS. Si les patients ne participent pas, nous ne pouvons pas obtenir cette prochaine génération de traitements.
RECHERCHE : Aidez à valider les échelles et les mesures de résultats qui peuvent aller au-delà des crises, afin que les nouvelles thérapies puissent montrer qu’elles sont meilleures que les thérapies actuelles contre les crises (je pense que nous faisons déjà cela bien avec les études U01 et CANDID et avec ELPIS).
ÉDUQUER les familles sur les thérapies géniques : Qu’est-ce que nous pouvons raisonnablement attendre, à quoi ressemble le parcours d’un essai pour une thérapie génique…
SUPPORT: Certains défis que nous ne pouvons pas résoudre mais que nous pouvons peut-être influencer sont de faire comprendre aux régulateurs ce dont nous avons besoin pour les essais cliniques de thérapie génique, et aussi le problème du prix des thérapies géniques.
RECHERCHE : Également au-delà de notre portée mais où nous pouvons rejoindre des chercheurs et d’autres communautés, il y a le problème de trouver un moyen de rendre les thérapies géniques redosables. Si nous savons que nous avons une deuxième chance, et qu’il ne s’agit pas seulement d’un objectif unique, cela facilitera la participation des gens aux essais et l’exécution de ces essais par les entreprises. Un moyen par lequel nous pourrions aider serait, par exemple, d’organiser un atelier ou une session au prochain Forum sur le côté immunitaire de la thérapie génique et comment pouvoir un jour redoser les patients.
Je vais ajouter deux choses qu’ils n’ont pas dites mais qui, selon moi, sont des rôles importants que la communauté joue également pour obtenir de nouveaux traitements :
RECHERCHE/COMMUNAUTÉ : J’ai remarqué que plusieurs des présentations concernaient des projets de recherche qui avaient initialement été financés par certains des groupes de patients nationaux, comme le Canada, l’Italie et l’Espagne. Cela montre que financer la recherche est un autre rôle important de la communauté des patients qui peut initier la construction d’une montagne avec le premier grain de sable. Je pense que c’est une fonction très importante des groupes de patients également, de financer la recherche sur le CDD dans leurs pays.
COMMUNAUTÉ : Nous devons vraiment trouver plus de patients. Il est clair qu’il y a plus de patients vivant avec le CDD qui ne connaissent pas encore leurs diagnostics que ceux qui ont déjà le bon diagnostic. Un patient non diagnostiqué est une personne qui pourrait être dans le mauvais traitement, qui manquera tous ces essais et qui ne pourra pas nous aider à résoudre les questions scientifiques (y compris l’épidémiologie précise de la maladie). Je crois que cela doit être abordé à un niveau national, donc je l’ajoute à nos listes de choses à faire !
6 – La communauté des patients : appartenance, croyance et action

Le Forum s’ouvre et se clôt traditionnellement avec la voix du patient, et cette année, il a débuté avec Lily Howard qui nous a fait part de son expérience en tant que sœur de Harper, une petite fille atteinte de CDD. Lily a parlé d’isolement et de maturité forcée, et de se sentir différente des autres enfants et incapable de se connecter. C’est pourquoi elle a créé un événement pour les frères et sœurs, afin qu’ils puissent créer un sentiment d’appartenance.
Lors du grand dîner de gala, le prix du patient a été décerné à Ana Carolina et Andreas Borg, les parents de la petite Siena, qui ont parlé du choc initial du diagnostic, de la découverte d’un monde qu’ils ne savaient pas exister, puis de la recherche d’un but. Je partagerai une belle phrase d’Andreas : « tous les problèmes solvables peuvent être résolus si suffisamment de personnes talentueuses mettent leur énergie dans ces problèmes », et une d’Ana : « nous cherchons toujours des héros, et je suis fier d’élever le mien ». C’est la nuit magique du Forum où nous finissons tous par pleurer tout en croyant en un avenir merveilleux que nous pouvons construire.
Pour clore le Forum, le président sortant de la CDKL5 Alliance, Heike, a de nouveau évoqué la nécessité d’unité au sein de la communauté des patients et a partagé les points forts des travaux de l’année écoulée par chaque groupe de patients de l’Alliance. Il nous a également rappelé que nous devrions essayer d’améliorer la qualité de vie, pas seulement nous concentrer sur les thérapies géniques, avec l’exemple de sa fille Valentina qui est passée de 3-4 crises par jour à 3-4 crises par mois dans un essai clinique, donc chaque petit effort que nous pouvons fournir compte beaucoup. Cet appel fait écho aux mots de Lily à l’ouverture du Forum, lorsqu’elle nous a dit que même les technologies d’assistance (pas même des médicaments) peuvent améliorer la qualité de vie des patients et de leurs familles. C’est un beau rappel qu’à la fin de la journée, nous traitons une personne, pas seulement un gène.
Enfin, Majid Jafar, co-fondateur de la Loulou Foundation, a clôturé le Forum en nous demandant à tous de nous retrouver à la réunion de la CDKL5 Alliance à Rome en juin 2025, et a annoncé que le prochain Forum CDKL5 reviendrait à Boston les 27 et 28 octobre 2025. Et il nous a laissé avec un appel à l’action : « nous sommes allés si loin… et il reste encore tant à faire. Faisons-le ».
Ainsi, nous retournons au travail avec nos têtes pleines d’idées et nos cœurs remplis d’amis. J’ai hâte de tous vous revoir à Rome et à Boston l’année prochaine.
Ana Mingorance, PhD
Avertissement : Ceci est mon propre résumé et mes principaux enseignements, et non un texte officiel sur le Forum par la Loulou Foundation. J’écris ces textes en pensant aux parents des personnes atteintes de CDD, donc excusez également mon manque de précision technique dans certaines parties.
